Review Slide
Medical Laboratory Technology Slideshow: Budi’s trip to Surabaya, Java, Indonesia was created by TripAdvisor. See another Surabaya slideshow. Take your travel photos and make a slideshow for free.
menu
MIKROBIOLOGI UNTUK TEHNISI KESEHATAN
- Oleh : Budi Raharja
- Surabaya, Jawa Timur, Indonesia
- Kumpulan informasi, pengetahuan dan tautan kami di BLOG "Mikrobiologi untuk Tehnisi Kesehatan" semoga bisa dijadikan sumber informasi dan referensi. serta membangkitkan inspirasi. Saat ini kami sudah banyak menerima permintaan konsultasi dan layanan pemeriksaan laboratorium klinik khususnya pemeriksaan mikrobiologi dan histopatologi dan pemeriksaan medis langka lainnya yang memerlukan prosedur rumit dan pengalaman serta skill yang cukup. Kami telah banyak memberikan advis dan membangun afiliasi sinergis dengan Laboratorium klinik/medis baik Swasta, unit laboratorium di RS. swasta maupun RS. milik Pemerintah. Bila sejawat memerlukan kemitraan dengan kami silakan menghubungi : "MicroTech" atau "MediTech", Telp : 082 242 743 284 NON STOP 24 jAM TERMASUK HARI RAYA /HARI LIBUR, SAMPEL BISA KAMI AMBIL, HASIL KAMI ANTAR. "Kami Melayani Anda untuk menjadi yang Terbaik"
Senin, 30 Agustus 2010
Minggu, 29 Agustus 2010
Microincinerator, bagaimana menggunakannya?
Cara Menggunakan Microincinerator di Laboratorium Mikrobiologi
Fiksasi smear: Spesimen bakteri pada slide mikroskop disebut smear. Dibuat dengan menggunakan contoh bakteri yang diperoleh dengan inokulasi loop disuspensikan dengan air atau larutan garam fisiologis pada permukaan slide mikroskop. Bakteri sangat kecil dan pada dasarnya tidak berwarna, suntuk itu smear bakteri harus diwarnai agar tampak apabila dilihat melalui mikroskop.
Tujuan fiksasi (pemanasan) adalah untuk merekatkan smear supaya tidak hilang selama pewarnaan, tempelkan slide di atas microincinerator (lihat foto di bawah). Dengan menempatkan slide smear bakteri pada platform slide selama beberapa menit, bakteri akan mati dan melekat pada slide sehingga tidak akan tercuci selama pewarnaan.
Microincinerator, juga dikenal sebagai bactoincinerator, adalah sebuah perangkat yang digunakan di laboratorium mikrobiologi untuk mensterilkan instrumen.
Sterilisasi instrumen ini terdiri dari tabung keramik dengan logam dan dikelilingi oleh cekungan di bagian tengah. Ketika terpasang dan dihidupkan, microincinerator bisa mencapai suhu 800 derajat celcius, lebih dari cukup untuk membakar bahan organik pada loop inokulasi.
Mengapa Microincinerator Dibutuhkan?
Dalam laboratorium mikrobiologi kontaminasi bahan steril harus dihindari, ini hal yang sulit karena bakteri dan spora jamur tersebar di lingkungan sekitar . Menghindari kontaminasi membutuhkan penggunaan teknik aseptik serta terus-menerus memperhatikan setiap tindakan yang dilakukan di laboratorium mikrobiologi.
Bakteri seringkali ditransfer menggunakan loop inokulasi (alias ose). Alat ini pada dasarnya adalah kawat dengan lingkaran kecil di salah satu ujung dan gagang di ujung lainnya. Ose terbuat dari logam, dapat digunakan berulang kali dan kemudian resterilized dalam nyala api atau microincinerator. Menyalakan api berpotensi kebakaran sedangkan Microincinerator sangat aman.
Dalam laboratorium mikrobiologi kontaminasi bahan steril harus dihindari, ini hal yang sulit karena bakteri dan spora jamur tersebar di lingkungan sekitar . Menghindari kontaminasi membutuhkan penggunaan teknik aseptik serta terus-menerus memperhatikan setiap tindakan yang dilakukan di laboratorium mikrobiologi.
Bakteri seringkali ditransfer menggunakan loop inokulasi (alias ose). Alat ini pada dasarnya adalah kawat dengan lingkaran kecil di salah satu ujung dan gagang di ujung lainnya. Ose terbuat dari logam, dapat digunakan berulang kali dan kemudian resterilized dalam nyala api atau microincinerator. Menyalakan api berpotensi kebakaran sedangkan Microincinerator sangat aman.
Bagaimana menggynakan Microincinerator ?
Ada dua tujuan utama yang insinerator-bacto digunakan dalam praktek di laboratorium:mikrobiologi
1. mensterilkan loop inokulasi
2. fiksasi smear bakteri
Ada dua tujuan utama yang insinerator-bacto digunakan dalam praktek di laboratorium:mikrobiologi
1. mensterilkan loop inokulasi
2. fiksasi smear bakteri
Untuk mensterilkan ose, masukkan ujung lingkar ose ke cekungan microincinerator beberapa detik, sampai bagian dari kawat inokulasi yang sedang disterilkan bersinar merah. Kemudian tarik loop dari insinerator, seketika itu akan berhenti memerah, dan dalam waktu 20 detik atau lebih, akan cukup dingin untuk digunakan.
Fiksasi smear: Spesimen bakteri pada slide mikroskop disebut smear. Dibuat dengan menggunakan contoh bakteri yang diperoleh dengan inokulasi loop disuspensikan dengan air atau larutan garam fisiologis pada permukaan slide mikroskop. Bakteri sangat kecil dan pada dasarnya tidak berwarna, suntuk itu smear bakteri harus diwarnai agar tampak apabila dilihat melalui mikroskop.
Tujuan fiksasi (pemanasan) adalah untuk merekatkan smear supaya tidak hilang selama pewarnaan, tempelkan slide di atas microincinerator (lihat foto di bawah). Dengan menempatkan slide smear bakteri pada platform slide selama beberapa menit, bakteri akan mati dan melekat pada slide sehingga tidak akan tercuci selama pewarnaan.
Sabtu, 28 Agustus 2010
PEWARNAAN BAKTERI
Pewarnaan Endospora bakteri
Uji diferensial untuk mengidentifikasi Bakteri Genus Bacillus & Clostridium
Pewarnaan endospora B. Subtilis (Spora Green) - Y tambe Wiki
Pewarnaan endospora menggunakan serangkaian pewarna, zat Malachite hijau untuk endospores dan zat safranin warna pink untuk sel vegetatif.
Sebelum membahas prosedur untuk pewarnaan endospores, penting untuk mengetahui sifat endospora
John Tyndall, orang Irlandia kelahiran Inggris pada abad ke-17 , seorang fisikawan yang membuat banyak kontribusi untuk ilmu pengetahuan, salah satunya adalah penemuan bahwa beberapa mikroba ada dalam dua bentuk:
1. bentuk tahan panas (endospores)
2. bentuk peka panas (sel-sel hidup vegetatif)
Tyndall menemukan bahwa butuh pemanasan lama atau bertahap untuk menghancurkan bentuk mikroba yang tahan panas. Hasil dari penelitian ini adalah metode sterilisasi dengan memanaskan ke titik didih pada 2 - 3 hari berturut-turut ("Tyndallization").
"Tyndallization" berguna untuk sterilisasi media pertumbuhan dan situasi lain di mana otoklaf ( instrumen yang menggunakan panas dan tekanan untuk mensterilkan) tidak tersedia
Apakah endospora itu?
Endospores diproduksi oleh beberapa jenis bakteri terutama genus Clostridium dan Bacillus. Struktur pelindung ini dibuat untuk menanggapi kondisi lingkungan yang ekstrim (seperti suhu tinggi, pengeringan, bahan kimia, perubahan pH dan kekurangan makanan).melalui proses yang dikenal sebagai sporulasi
Dalam, bentuk menyandang endospora, bakteri tidak dapat memetabolisme atau mereproduksi, tetapi mirip seperti benih tanaman. Ketika kondisi lingkungan kembali menjadi menguntungkan, bakteri kembali ke bentuk aktif (sel vegetatif).
Pewarnaan Endospores bakteri
Endospora sulit diwarnai dengan metode Gram. Untuk pewarnaan endspores, perlu dilakukan pemanasan supaya cat malachite hijau bisa masuk ke dalam spora , seperti halnya pada pewarnaan Basil Tahan Asam dimana cat carbol fuschsin harus dipanaskan untuk bisa menembus lapisan lilin asam mycolic dari Mycobacterium .
Skema prosedur pengecatan Spora Schaeffer Fulton
Uji diferensial untuk mengidentifikasi Bakteri Genus Bacillus & Clostridium
Pewarnaan endospora B. Subtilis (Spora Green) - Y tambe Wiki
Pewarnaan endospora menggunakan serangkaian pewarna, zat Malachite hijau untuk endospores dan zat safranin warna pink untuk sel vegetatif.
Sebelum membahas prosedur untuk pewarnaan endospores, penting untuk mengetahui sifat endospora
John Tyndall, orang Irlandia kelahiran Inggris pada abad ke-17 , seorang fisikawan yang membuat banyak kontribusi untuk ilmu pengetahuan, salah satunya adalah penemuan bahwa beberapa mikroba ada dalam dua bentuk:
1. bentuk tahan panas (endospores)
2. bentuk peka panas (sel-sel hidup vegetatif)
Tyndall menemukan bahwa butuh pemanasan lama atau bertahap untuk menghancurkan bentuk mikroba yang tahan panas. Hasil dari penelitian ini adalah metode sterilisasi dengan memanaskan ke titik didih pada 2 - 3 hari berturut-turut ("Tyndallization").
"Tyndallization" berguna untuk sterilisasi media pertumbuhan dan situasi lain di mana otoklaf ( instrumen yang menggunakan panas dan tekanan untuk mensterilkan) tidak tersedia
Apakah endospora itu?
Endospores diproduksi oleh beberapa jenis bakteri terutama genus Clostridium dan Bacillus. Struktur pelindung ini dibuat untuk menanggapi kondisi lingkungan yang ekstrim (seperti suhu tinggi, pengeringan, bahan kimia, perubahan pH dan kekurangan makanan).melalui proses yang dikenal sebagai sporulasi
Dalam, bentuk menyandang endospora, bakteri tidak dapat memetabolisme atau mereproduksi, tetapi mirip seperti benih tanaman. Ketika kondisi lingkungan kembali menjadi menguntungkan, bakteri kembali ke bentuk aktif (sel vegetatif).
Pewarnaan Endospores bakteri
Endospora sulit diwarnai dengan metode Gram. Untuk pewarnaan endspores, perlu dilakukan pemanasan supaya cat malachite hijau bisa masuk ke dalam spora , seperti halnya pada pewarnaan Basil Tahan Asam dimana cat carbol fuschsin harus dipanaskan untuk bisa menembus lapisan lilin asam mycolic dari Mycobacterium .
Skema prosedur pengecatan Spora Schaeffer Fulton
Protokol pewarnaan diferensial endospores dan sel vegetatif adalah sebagai berikut:
- Letakkan slide bakteri di atas bak air yang dipanaskan
- Genangi slide dengan larutan malachit green yang sudah disaring, (sebagai pewarna utama), biarkan posisi
slide tetap di atas bak air panas (seperti dikukus) selama 5 menit, tambahkan larutan malachit jika mulai
mengering.
- Angkat slide dari bak air dan bilas dengan air sampai tidak ada lagi pewarna yang tinggal.
- Genangi slide dengan safrinin (counterstain) selama 20 detik dan kemudian bilas.
- Lihat slide dengan mikroskop cahaya.(pembesaran 1000xTM, menggunakan minyak immersi)
Hasil Pengamatan :
Endospores akan tampak hijau, karena mempertahankan warna utama, Malachite hijau . Sel-sel vegetatif akan terlihat merah muda, karena menyerap safrinin.
Problem Interpretasi pengecatan endospora
Perlu dicatat bahwa setiap goresan kecil pada slide juga dapat terlihat hijau. Segala sesuatu pada slide yang terlihat hijau belum tentu sebuah endospora. Endospores itu kecil dan biasanya oval., adapun gumpalan hijau besar atau tidak teratur pada slide dapat dikatakan artefak.
Pewarnaan Ziehl Neelsen
Uji diferensial untuk Mengidentifikasi Bakteri Mycobacterium dan Nocardia
Bakteri Tahan Asam (pink) dan bakteri Tidak Tahan Asam (biru)
Mycobacterium dan Nocardia adalah penyebab penyakit menular, seperti tuberkulosis, kusta dan infeksi paru-paru serta kulit.lainnya. Oleh karena itu, jelas penting untuk dapat mengidentifikasi secara akurat anggota genus ini.
Dinding Sel mikobakteri dan Nocardia
Bakteri Mycobacterium dan Nocardia memiliki dinding sel yang tidak biasa , yang licin dan sukar ditembus karena adanya asam mycolic dan sejumlah besar asam lemak, lilin, dan lipid kompleks. Organisme ini sangat tahan terhadap desinfektan, pengeringan dan sulit untuk diwarnai dengan pewarna berbasis air seperti Gram.
Pewarnaan Tahan Asam memerlukan teknik pewarnaan khusus yang menggunakan panas untuk menambah daya tembus cat masuk ke dalam dinding sel lilin bakteri
Membuat preparat (mear) yang akan dicat Tahan Asam.
Smear adalah sampel bakteri tersuspensi dalam jumlah kecil air pada slide. sampel itu kemudian dikeringkan dengan panas. Panas membunuh bakteri dan melekatkan sampel ke slide sehingga tidak mudah terbilas..
Gambar : prosedur pewarnaan tahan asam
Pengecatan BTA Ziehl Neelsen
Maksud : Cara mengidentifikasi Bakteri Tahan Asam (BTA) menggunakan metode pengecatan Ziehl
Nielsen
Tujuan : Diagnosis
Sampel : sputum, lesi, Swab, pus, urine, darah, faeces, liquor, pleura, ascites,dll.
Alat :
- Lampu Spirtus/bunzen
- Obyek glass
- Rak pengecatan
- Ose
- Pipet pasteur
- mikroskop
Reagen :
1. Carbol fuchsin :
- Basic fuchsin 3,0 gr
- Etanol/methanol 100 ml
- Kristal phenol 45 gr
- Aquadest 900 ml
2. larutan dekolorisasi :
- HCl pekat 30 ml
- Etanol 970 ml
3. Warna pembandung :
- Methylen blue khlorida 30 ml
- Air suling/aquadest 1000 ml
Cara kerja :
Protokol untuk pewarnaan tahan asam adalah sebagai berikut:
- Letakkan slide di atas bak air panas
- Genangi slide dengan carbol fuchsin (pewarna utama)
- Biarkan slide di atas bak air yang dipanaskan selama 3 - 5 menit, tambahkan larutan carbol fuchsin jika
mulai mengering.
- Angkat slide dan bilas sampai bersih dan tak ada lagi cat yang terbawa air bilasan.
- Tuangi slide dengan decolorizer, Asam Alkohol, selama 10 - 15 detik dan kemudian bilas.
- Tuangi slide dengan counterstain, Metilen blue, selama satu menit dan kemudian bilas.
- Keringkan slide. Sekarang siap untuk ditampilkan di bawah rmkroskop menggunakan minyak (1000x)
Interpretasi
Sel Tahan Asam akan berwarna merah muda, karena menyerap carbol fuschion dengan bantuan pemanasan Sel Non Tahan Asam, (bakteri yang tidak memiliki dinding sel lilin) akan berwarna biru, s
Referensi :
Bauman, R. (2005) Mikrobiologi.
Pewearnaan Gram
Uji Identifikasi dan klasifikasi bakteri Gram-positif dan Gram-negatif
Pengantar
Setelah mikroba diakui sebagai sumber penyakit menular, iperlukan suatu metode untuk mendeteksi dan mengidentifikasi bentuk-bentuk kehidupan mikroba. Namun mikroba tidak berwarna dan sulit untuk dilihat.
Pada 1800-an, Kristen Gram, ahli bakteriologi Denmark, telah mengembangkan teknik untuk pewarnaan bakteri yang masih banyak digunakan sampai saat ini yaitu Gram stain. Pewarnaan Gram penting untuk mengklasifikasikan bakteri ke dalam kelompok Gram positip atau Gram negatip. Dalam pengecatan Gram, bakteri disebut Gram-positif bila berwarna ungu dan Gram-negatif. bila berwarna pink, Pewarnaan Gram adalah uji diferensial yang menggunakan dua zat warna untuk membedakan antara dua tipe dasar dinding sel bakteri.
Berikut sedikit paparan bagaimana cara pewarnaan Gram (Modifikasi) dan Interpretasinya, semoga bermanfaat :
Pewearnaan Gram
Uji Identifikasi dan klasifikasi bakteri Gram-positif dan Gram-negatif
Pengantar
Setelah mikroba diakui sebagai sumber penyakit menular, iperlukan suatu metode untuk mendeteksi dan mengidentifikasi bentuk-bentuk kehidupan mikroba. Namun mikroba tidak berwarna dan sulit untuk dilihat.
Pada 1800-an, Kristen Gram, ahli bakteriologi Denmark, telah mengembangkan teknik untuk pewarnaan bakteri yang masih banyak digunakan sampai saat ini yaitu Gram stain. Pewarnaan Gram penting untuk mengklasifikasikan bakteri ke dalam kelompok Gram positip atau Gram negatip. Dalam pengecatan Gram, bakteri disebut Gram-positif bila berwarna ungu dan Gram-negatif. bila berwarna pink, Pewarnaan Gram adalah uji diferensial yang menggunakan dua zat warna untuk membedakan antara dua tipe dasar dinding sel bakteri.
1. Pengecatan Gram
Maksud : adalah tata cara laboratorium untuk mengindentifikasi bakteri menggunakan metode
pengecatan Gram.
Tujuan : Diagnosis
Sampel : Swab, pus, urine, darah faeces, liquor, pleura, ascites, sputum, bahab usapan, sekret,dll.
Alat :
- Lampu spiritus/bunzen
- Pipet Pasteur
- Obyek Glass
- Rak pengecatan
- Ose
- Mikroskop
Reagen :
1. Larutan Gram A (Carbol Gentian Violet) :
a. Gentian Violet 1 gr
b. Alkohol 96% 10 ml
c. Phenol Kristal 1 gr
d. Aquadest 90 ml
2. Larutan Gram B (lugol)
a. Yodium 1 gr
b. Kalium Yodida 2 gr
c. Aquadest 300 ml
3. Larutan gram C (Alkohol 96%)
4. Larutan Gram D ( Basic fuchsin 1%)
a. Basic Fuchsin 1 gr
b. Aquadest 100 ml
Berikut sedikit paparan bagaimana cara pewarnaan Gram (Modifikasi) dan Interpretasinya, semoga bermanfaat :
Prosedur operasi standar
Prosedur operasi standar
Tunggu tulisan berikutnya....
Prosedur operasi standar (POS) ,(Bahasa Inggris: standard operating procedure, SOP) adalah seperangkat instruksi yang memiliki kekuatan sebagai suatu petunjuk . Hal ini mencakup tindakan yang memiliki suatu prosedur pasti atau terstandardisasi, tanpa kehilangan keefektifannya. Setiap sistem manajemen kualitas yang baik selalu didasari oleh POS.
Prosedur adalah serangkaian aksi yang spesifik, tindakan atau operasi yang harus dijalankan dengan cara yang sama agar selalu memperoleh hasil yang sama dari keadaan yang sama (contohnya prosedur kesehatan dan keselamatan kerja). Lebih tepatnya, prosedur adalah rangkaian aktivitas, tugas-tugas, langkah-langkah, keputusan-keputusan, perhitungan-perhitungan dan proses-proses, yang dijalankan melalui serangkaian pekerjaan untuk menghasilkan suatu tujuan yang diinginkan, suatu produk atau sebuah akibat.
Jumat, 27 Agustus 2010
Neisseriae :
Neisseriae Patogen: Gonore, Oftalmia dan Meningitis meningokokus
Pengenalan
Gambar 3. Patogenesis gonore tanpa komplikasi menurut Morse di Baron, Bab 14, Neisseria, Branhamella, Moraxella dan Eikenella
Neisseria meningitidis
Struktur dan Klasifikasi
Yang membedakan fitur struktural antara N.gonorrhoeae dan N. meningitidis adalah adanya kapsul polisakarida yang bersifat antiphagocytic dan merupakan faktor virulensi penting.
Pengenalan
Keluarga Neisseriaceae terdiri dari empat belas genera (Bergey's 2001) adalah bakteri aerobik-Gram negatif. Neisseriaceae meliputi Neisseria, Chromobacterium, Kingella, dan Aquaspirillum. Genus Neisseria berisi dua patogen penting pada manusia, N. gonorrhoeae dan N. meningitidis. N. gonorrhoeae penyebab gonore, dan N. meningitidis adalah penyebab meningitis meningokokus. Infeksi N. gonorrhoeae memiliki prevalensi tinggi dan kematian rendah, sedangkan infeksi N. meningitidis memiliki prevalensi rendah dan kematian tinggi.
Infeksi Neisseria gonorrhoeae ditularkan melalui kontak seksual dan biasanya mempengaruhi selaput lendir dari saluran kencing pada laki-laki juga endoserviks dan urethra pada wanita, meskipun mungkin infeksi dapat menyebar ke berbagai jaringan. . Banyak orang normal menjadi pembawa Neisseria meningitidis di saluran pernapasan bagian atas, tapi Neisseria gonorrhoeae tidak pernah sebagai bagian dari flora normal dan hanya ditemukan setelah kontak seksual dengan orang yang terinfeksi (atau kontak langsung, dalam kasus infeksi pada bayi baru lahir).
N. gonorrhoeae sering disebut sebagai gonokokus "", sedangkan N. meningitidis dikenal sebagai meningokokus "" dan salah satu bentuk penyakit yang disebabkan disebut meningococcemia.
Pewarnaan Gram dari biakan murni pewarnaan Gram dari eksudat
Gambar 1. Neisseria gonorrhoeae
Neisseria gonorrhoeae adalah Bakteri kokus Gram-negatif , diameter 0,6-1,0 μm , biasanya terlihat berpasangan, sisi yang saling berdekatan rata . Organisme ini sering ditemukan intraseluler di leukosit polymorphonuclear (neutrofil) dari gonorrhea pada eksudat (Gambar 1 kanan).
Neisseria gonorrhoeae. memiliki membran luar terdiri dari protein, fosfolipid, dan lipopolisakarida (LPS). . LPS neisserial disebut sebagai lipooligosaccharide (LOS).
N. gonorrhoeae adalah organisme yang relatif rapuh, rentan terhadap perubahan suhu, pengeringan, lampu uv, dan kondisi lingkungan lainnya. Strain dari N. gonorrhoeae mudah tumbuh pada media yang mengandung hemoglobin, NAD, ekstrak ragi dan suplemen lain yang dibutuhkan Biakan ditanam pada 35-36 derajat dalam suasana penambahan 3 -10% CO 2.
Infeksi yang disebabkan N. gonorrhoeae
Penyakit gonore adalah jenis uretritis spesifik yang hampir selalu melibatkan selaput lendir dari saluran kencing, mengakibatkan debit nanah berlebihan , lebih jelas pada pria dibandingkan pada wanita.
Penyakit gonore adalah jenis uretritis spesifik yang hampir selalu melibatkan selaput lendir dari saluran kencing, mengakibatkan debit nanah berlebihan , lebih jelas pada pria dibandingkan pada wanita.
Yang pertama menggunakan "istilah" gonore adalah Galen pada abad kedua, artinya aliran "benih". Penyakit Gonore pernah dikacaukan dengan sifilis.. Paracelsus (1530) berpikir bahwa gonore merupakan gejala awal sifilis. Kebingungan semakin tinggi oleh kesalahan dokter Inggris klasik , John Hunter, pada tahun 1767. Hunter sengaja menginokulasi dirinya dengan nanah, dari pasien dengan gejala gonore dan akhirnya memberikan dirinya sifilis! Agen penyebab gonore, Neisseria gonorrhoeae, pertama kali digambarkan oleh A. Neisser pada tahun 1879 dalam eksudat dari kasus gonore. Organisme ditumbuhkan dalam kultur murni pada 1885, dan hubungan etiologi terhadap penyakit manusia kemudian dipraktekan dengan menggunakan sukarelawan manusia dalam rangka memenuhi persyaratan eksperimental Postulat Koch.
Ifeksi Gonorrheal pada umumnya terbatas pada permukaan mukosa superfisial epitel kolumnar. Daerah yang paling sering terlibat adalah uretra, leher rahim, rektum, faring, dan konjungtiva. Epitel skuamosa, vagina dewasa, tidak rentan terhadap infeksi oleh N. gonorrhoeae. Namun, epitel vagina praremaja, yang belum keratinisasi akibat pengaruh estrogen, mungkin terinfeksi. Oleh karena itu, gonore pada anak perempuan muda dapat berupa vulvovaginitis mukosa yang biasanya ditandai dengan keluarnya cairan bernanah.
Gonore, merupakan infeksi piogenik, menyebabkan inflamasi pada selaput lendir uretra anterior. Gejala yang paling umum adalah keluarnya cairan bernanah yang berlebihan., disuria (kesulitan buang air kecil) . Peradangan pada jaringan uretra terlihat kemerahan, bengkak panas, dan nyeri. Ada rasa terbakar dan rasa sakit pada saat buang air kecil.
Infeksi endoserviks adalah bentuk paling umum dari gonorrhea tanpa komplikasi pada wanita. infeksi tersebut biasanya ditandai dengan cairan vagina dan kadang-kadang dengan disuria. Sekitar 50% wanita dengan infeksi serviks tidak menunjukkan gejala. Asimtomatik infeksi juga terjadi pada laki-laki, . Pria dengan uretritis asimtomatik merupakan reservoir yang penting dalam penularan dan akan meningkatkan risiko komplikasi.
Pada pria, organisme dapat menyerang prostat menyebabkan prostatitis, atau ke testis menghasilkan orkitis. Pada perempuan, serangan ke serviks dapat meluas melalui rahim ke tuba falopi menyebabkan salpingitis, atau ke ovarium menghasilkan ovaritis. Komplikasi ke testis, tabung fallopi atau ovarium dapat mengakibatkan kemandulan. Kadang-kadang, infeksi meluas. Yang paling umum bentuk infeksi meluas adalah sindrom artritis-dermatitis, endokarditis dan meningitis.
Infeksi Rektal (proktitis) dengan N. gonorrhoeae terjadi pada sekitar sepertiga dari wanita dengan infeksi serviks,. paling sering akibat dari autoinoculation dari serviks dan jarang timbul gejala Rektal pada pria homoseksual biasanya hasil dari hubungan seks anal.
Infeksi mata oleh N. gonorrhoeae menyebabkan konsekuensi serius timbulnya jaringan parut kornea atau perforasi. pada mata (neonatorum Oftalmia), terjadi paling sering pada bayi baru lahir yang terkena sekresi terinfeksi di jalan lahir. Meneteskan cairan perak nitrat atau antibiotik pada mata bayi yang baru lahir adalah untuk mencegah infeksi okular oleh N. gonorrhoeae.
Ifeksi Gonorrheal pada umumnya terbatas pada permukaan mukosa superfisial epitel kolumnar. Daerah yang paling sering terlibat adalah uretra, leher rahim, rektum, faring, dan konjungtiva. Epitel skuamosa, vagina dewasa, tidak rentan terhadap infeksi oleh N. gonorrhoeae. Namun, epitel vagina praremaja, yang belum keratinisasi akibat pengaruh estrogen, mungkin terinfeksi. Oleh karena itu, gonore pada anak perempuan muda dapat berupa vulvovaginitis mukosa yang biasanya ditandai dengan keluarnya cairan bernanah.
Gonore, merupakan infeksi piogenik, menyebabkan inflamasi pada selaput lendir uretra anterior. Gejala yang paling umum adalah keluarnya cairan bernanah yang berlebihan., disuria (kesulitan buang air kecil) . Peradangan pada jaringan uretra terlihat kemerahan, bengkak panas, dan nyeri. Ada rasa terbakar dan rasa sakit pada saat buang air kecil.
Infeksi endoserviks adalah bentuk paling umum dari gonorrhea tanpa komplikasi pada wanita. infeksi tersebut biasanya ditandai dengan cairan vagina dan kadang-kadang dengan disuria. Sekitar 50% wanita dengan infeksi serviks tidak menunjukkan gejala. Asimtomatik infeksi juga terjadi pada laki-laki, . Pria dengan uretritis asimtomatik merupakan reservoir yang penting dalam penularan dan akan meningkatkan risiko komplikasi.
Pada pria, organisme dapat menyerang prostat menyebabkan prostatitis, atau ke testis menghasilkan orkitis. Pada perempuan, serangan ke serviks dapat meluas melalui rahim ke tuba falopi menyebabkan salpingitis, atau ke ovarium menghasilkan ovaritis. Komplikasi ke testis, tabung fallopi atau ovarium dapat mengakibatkan kemandulan. Kadang-kadang, infeksi meluas. Yang paling umum bentuk infeksi meluas adalah sindrom artritis-dermatitis, endokarditis dan meningitis.
Infeksi Rektal (proktitis) dengan N. gonorrhoeae terjadi pada sekitar sepertiga dari wanita dengan infeksi serviks,. paling sering akibat dari autoinoculation dari serviks dan jarang timbul gejala Rektal pada pria homoseksual biasanya hasil dari hubungan seks anal.
Infeksi mata oleh N. gonorrhoeae menyebabkan konsekuensi serius timbulnya jaringan parut kornea atau perforasi. pada mata (neonatorum Oftalmia), terjadi paling sering pada bayi baru lahir yang terkena sekresi terinfeksi di jalan lahir. Meneteskan cairan perak nitrat atau antibiotik pada mata bayi yang baru lahir adalah untuk mencegah infeksi okular oleh N. gonorrhoeae.
Patogenesis
Gonorrhea pada orang dewasa hampir selalu ditularkan melalui hubungan seksual. Bakteri memasuki kolumnar sel epitel, penetrasi, dan memperbanyak diri pada membran basement. Melekatkan fimbriae dan protein opa (P. II) .
Neisseria gonorrhoeae dapat menghasilkan satu atau beberapa membran luar protein yang disebut protein Opa (P. II) . Protein ini biasanya ditemukan pada sel-sel dari koloni yang memiliki fenotipe buram unik yang disebut O +. Pada waktu tertentu, bakteri dapat mengekspresikan nol, satu, atau beberapa Opa protein yang berbeda , dan masing-masing strain memiliki 10 atau lebih gen untuk Opa berbeda.
Rmp (P. III) adalah protein membran luar ditemukan pada semua strain N. gonorrhoeae. Ia tidak mengalami variasi antigenik dan ditemukan dalam sebuah kompleks dengan Por dan LOS., sebagian antigen homologi dengan protein OmpA Escherichia coli Rmp. untuk Antibodi , baik yang disebabkan oleh infeksi neisserial atau kolonisasi dengan E. coli, cenderung untuk memblokir antibodi bakterisidal yang diarahkan terhadap Por dan LOS. Bahkan, anti-Rmp antibodi dapat meningkatkan kerentanan terhadap infeksi oleh N. gonorrhoeae.
Selama infeksi, lipooligosaccharide bakteri (LOS) dan peptidoglikan dirilis oleh otolisis sel. Kedua polisakarida bakteri mengaktifkan komplemen jalur alternatif tuan rumah, sementara LOS juga merangsang faktor produksi nekrosis tumor (TNF) yang menyebabkan kerusakan sel. Neutrofil segera tertarik menuju situs dan memakan bakteri. Untuk alasan yang tidak diketahui, gonokokus banyak yang mampu bertahan dari fagosit, paling tidak sampai neutrofil sendiri mati dan melepaskan bakteri yang tertelan.
Neisserial LOS memiliki efek mendalam pada virulensi dan patogenesis N. gonorrhoeae. LOS. gonokokal menghasilkan kerusakan mukosa dalam organ tabung fallopi dan melepas enzim, seperti protease dan phospholipases Jadi, LOS gonokokal tampaknya memiliki peran tidak langsung dalam mediasi kerusakan jaringan. LOS gonokokal juga terlibat dalam perlawanan N. gonorrhoeae terhadap aktivitas bakterisida dari serum manusia
N. gonorrhoeae sangat efisien dalam memanfaatkan besi-transferin dalam pertumbuhan in vitro; banyak strain juga memanfaatkan besi terikat laktoferin. Kekhususan mengikat transferin dan laktoferin. ini dianggap, sebagai bakteri patogen manusia
Kadang-kadang, Neisseria gonorrhoeae masuk ke aliran darah menyebabkan bakteremia Asimtomatik infeksi dari uretra atau leher rahim biasanya sebagai sumber bakteremia. Strain N. gonorrhoeae yang menyebabkan penyebaran infeksi biasanya tahan bakterisida dan reaksi serum. Ini menjelaskan kemampuan mereka dalam bertahan sebagai bakteremia
Gonorrhea pada orang dewasa hampir selalu ditularkan melalui hubungan seksual. Bakteri memasuki kolumnar sel epitel, penetrasi, dan memperbanyak diri pada membran basement. Melekatkan fimbriae dan protein opa (P. II) .
Neisseria gonorrhoeae dapat menghasilkan satu atau beberapa membran luar protein yang disebut protein Opa (P. II) . Protein ini biasanya ditemukan pada sel-sel dari koloni yang memiliki fenotipe buram unik yang disebut O +. Pada waktu tertentu, bakteri dapat mengekspresikan nol, satu, atau beberapa Opa protein yang berbeda , dan masing-masing strain memiliki 10 atau lebih gen untuk Opa berbeda.
Rmp (P. III) adalah protein membran luar ditemukan pada semua strain N. gonorrhoeae. Ia tidak mengalami variasi antigenik dan ditemukan dalam sebuah kompleks dengan Por dan LOS., sebagian antigen homologi dengan protein OmpA Escherichia coli Rmp. untuk Antibodi , baik yang disebabkan oleh infeksi neisserial atau kolonisasi dengan E. coli, cenderung untuk memblokir antibodi bakterisidal yang diarahkan terhadap Por dan LOS. Bahkan, anti-Rmp antibodi dapat meningkatkan kerentanan terhadap infeksi oleh N. gonorrhoeae.
Selama infeksi, lipooligosaccharide bakteri (LOS) dan peptidoglikan dirilis oleh otolisis sel. Kedua polisakarida bakteri mengaktifkan komplemen jalur alternatif tuan rumah, sementara LOS juga merangsang faktor produksi nekrosis tumor (TNF) yang menyebabkan kerusakan sel. Neutrofil segera tertarik menuju situs dan memakan bakteri. Untuk alasan yang tidak diketahui, gonokokus banyak yang mampu bertahan dari fagosit, paling tidak sampai neutrofil sendiri mati dan melepaskan bakteri yang tertelan.
Neisserial LOS memiliki efek mendalam pada virulensi dan patogenesis N. gonorrhoeae. LOS. gonokokal menghasilkan kerusakan mukosa dalam organ tabung fallopi dan melepas enzim, seperti protease dan phospholipases Jadi, LOS gonokokal tampaknya memiliki peran tidak langsung dalam mediasi kerusakan jaringan. LOS gonokokal juga terlibat dalam perlawanan N. gonorrhoeae terhadap aktivitas bakterisida dari serum manusia
N. gonorrhoeae sangat efisien dalam memanfaatkan besi-transferin dalam pertumbuhan in vitro; banyak strain juga memanfaatkan besi terikat laktoferin. Kekhususan mengikat transferin dan laktoferin. ini dianggap, sebagai bakteri patogen manusia
Kadang-kadang, Neisseria gonorrhoeae masuk ke aliran darah menyebabkan bakteremia Asimtomatik infeksi dari uretra atau leher rahim biasanya sebagai sumber bakteremia. Strain N. gonorrhoeae yang menyebabkan penyebaran infeksi biasanya tahan bakterisida dan reaksi serum. Ini menjelaskan kemampuan mereka dalam bertahan sebagai bakteremia
Gambar 3. Patogenesis gonore tanpa komplikasi menurut Morse di Baron, Bab 14, Neisseria, Branhamella, Moraxella dan Eikenella
Bakteri Neisseria meningitidis, meningokokus, adalah identik dalam pewarnaan dan karakteristik morfologi dengan Neisseria gonorrhoeae,. Namun pada tingkat ultrastructural, N. meningitidis memiliki kapsul polisakarida antiphagocytic. N. meningitidis strain dikelompokkan berdasarkan polisakarida kapsuler mereka menjadi 12 serogrup, beberapa dibagi berdasarkan adanya protein membran luar dan antigen lipopolisakarida.
Neisseria meningitidis biasanya dibiakkan dari spesimen darah dalam media-pepton dalam ruang lembab yang mengandung 5-10% CO 2. Semua media harus dihangatkan sampai 37 derajat sebelum inokulasi karena organisme sangat rentan terhadap suhu di atas atau di bawah 37 derajat. Sifat ini agak unik di antara bakteri. Selain itu, organisme cenderung mengalami otolisis cepat setelah kematian, baik secara in vitro dan in vivo. Ini menjelaskan penyebaran lipopolisakarida (endotoksin) selama septikemia dan meningitis.
Organisme ini cenderung tinggal di nasofaring posterior manusia, dan manusia adalah satu-satunya host . Individu yang terjajah adalah pembawa patogen yang dapat menularkan penyakit kepada individu nonimmune. bakteri ini juga berkolono di nasofaring posterior pada tahap awal infeksi sebelum invasi meninges.
Neisseria meningitidis biasanya dibiakkan dari spesimen darah dalam media-pepton dalam ruang lembab yang mengandung 5-10% CO 2. Semua media harus dihangatkan sampai 37 derajat sebelum inokulasi karena organisme sangat rentan terhadap suhu di atas atau di bawah 37 derajat. Sifat ini agak unik di antara bakteri. Selain itu, organisme cenderung mengalami otolisis cepat setelah kematian, baik secara in vitro dan in vivo. Ini menjelaskan penyebaran lipopolisakarida (endotoksin) selama septikemia dan meningitis.
Organisme ini cenderung tinggal di nasofaring posterior manusia, dan manusia adalah satu-satunya host . Individu yang terjajah adalah pembawa patogen yang dapat menularkan penyakit kepada individu nonimmune. bakteri ini juga berkolono di nasofaring posterior pada tahap awal infeksi sebelum invasi meninges.
Struktur dan Klasifikasi
Yang membedakan fitur struktural antara N.gonorrhoeae dan N. meningitidis adalah adanya kapsul polisakarida yang bersifat antiphagocytic dan merupakan faktor virulensi penting.
Dua belas serogrup telah diidentifikasi (A, B, C, H, I, K, L, X, Y, Z, 29E, dan W135). Serogrup yang paling penting berhubungan dengan penyakit pada manusia adalah A, B, C, Y, dan W135. .
Radang selaput
Meningitis merujuk peradangan meninges otak atau sumsum tulang belakang. Meninges adalah salah satu dari tiga membran yang menyelubungi otak dan sumsum tulang belakang. Meningitis disebabkan oleh sejumlah bakteri dan virus yang berbeda. termasuk Haemophilus influenzae, Escherichia coli, Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, dan Neisseria meningitidis.
Marchiafava dan cello adalah yang pertama mengamati diplococci Gram-negatif dalam cairan cerebrospinal dari kasus meningitis pada 1884. Pada tahun 1887, Weichselbaum mengisolasi bakteri dari enam kasus meningitis
Radang selaput
Meningitis merujuk peradangan meninges otak atau sumsum tulang belakang. Meninges adalah salah satu dari tiga membran yang menyelubungi otak dan sumsum tulang belakang. Meningitis disebabkan oleh sejumlah bakteri dan virus yang berbeda. termasuk Haemophilus influenzae, Escherichia coli, Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, dan Neisseria meningitidis.
Marchiafava dan cello adalah yang pertama mengamati diplococci Gram-negatif dalam cairan cerebrospinal dari kasus meningitis pada 1884. Pada tahun 1887, Weichselbaum mengisolasi bakteri dari enam kasus meningitis
Patogenesis
Infeksi diawali dengan perlekatan bakteri ke sel epitel dan mukosa nasofaring orofaringeal, melewati sawar mukosa, dan memasuki aliran darah.
Bentuk paling ringan penyakit adalah penyakit bacteremic transien ditandai dengan demam dan malaise; gejala hilang secara spontan dalam 1 sampai 2 hari.. Yang paling serius adalah fulminan . Manifestasi meningitis meningokokus mirip dengan bakteri akut meningitis yang disebabkan oleh bakteri lain seperti Streptococcus pneumoniae, Haemophilus influenzae, dan E. coli,. demam menggigil, malaise, dan sakit kepala merupakan manifestasi infeksi biasa. Tanda-tanda peradangan meningeal juga muncul
Infeksi diawali dengan perlekatan bakteri ke sel epitel dan mukosa nasofaring orofaringeal, melewati sawar mukosa, dan memasuki aliran darah.
Bentuk paling ringan penyakit adalah penyakit bacteremic transien ditandai dengan demam dan malaise; gejala hilang secara spontan dalam 1 sampai 2 hari.. Yang paling serius adalah fulminan . Manifestasi meningitis meningokokus mirip dengan bakteri akut meningitis yang disebabkan oleh bakteri lain seperti Streptococcus pneumoniae, Haemophilus influenzae, dan E. coli,. demam menggigil, malaise, dan sakit kepala merupakan manifestasi infeksi biasa. Tanda-tanda peradangan meningeal juga muncul
Kamis, 26 Agustus 2010
Difteri
Difteri
Corynebacterium diphtheriae
Corynebacteria adalah bakteri Gram-positif, aerobik, nonmotile, berbentuk batang diklasifikasikan sebagai Actinobacteria. Corynebacteria membentuk karakteristik yang tidak teratur, mereka mengalami gertakan gerakan setelah pembelahan sel, yang membuat mereka ke dalam bentuk-bentuk karakteristik yang mirip huruf Cina atau pagar.
Genus Corynebacterium terdiri dari berbagai kelompok bakteri patogen termasuk pada hewan dan tanaman, serta saprophytes. Beberapa Corynebacteria merupakan bagian dari flora normal manusia, terdapay di hampir semua situs anatomi, terutama kulit dan mukosa hidung.. Spesies yang paling dikenal dan paling banyak dipelajari adalah Corynebacterium diphtheriae, agen penyebab dari penyakit difteri.
Gambar 1. Sel. Corynebacterium, penampilan ini disebabkan oleh adanya inklusi polifosfat yang disebut butiran metachromatic. Perhatikan juga susunan sel. "karakteristik huruf Cina- "
Difteri adalah penyakit saluran pernapasan atas yang ditandai dengan sakit tenggorokan, demam rendah, dan membran putih abu-abu (disebut pseudomembrane pada tonsil, faring, dan / atau rongga hidung. Toksin Difteri. diproduksi oleh C. diphtheriae, dapat menyebabkan miokarditis, polyneuritis, dan efek beracun sistemik lainnya. Penyebaran penyakit melalui kontak fisik langsung atau cairan pernapasan aerosol dari individu yang terinfeksi. Vaksin DPT. terbukti efektif menurunkan insiden penyakit difteri.
Difteri adalah penyakit yang serius, dengan tingkat kematian antara 5% dan 10%. Pada anak-anak di bawah 5 tahun dan orang dewasa lebih dari 40 tahun, tingkat kematian mungkin sebanyak 20%. Wabah, meskipun sangat jarang, masih terjadi di seluruh dunia, bahkan di negara-negara maju.
Sejarah dan Latar Belakang
Hippocrates memberikan penjelasan klinis pertama dari difteri pada abad ke-4 SM
Pada abad ke-17, epidemi difteri menyapu Eropa; di Spanyol penyakit dikenal sebagai " El garatillo " (Sang pencekik "), di Italia dan Sisilia dikenal sebagai" penyakit tenggorokan ".
Pada abad ke-18, penyakit ini mencapai koloni Amerika di mana, sekitar tahun 1735 sering kali, seluruh keluarga dalam beberapa minggu meninggal karena penyakit ini .
Bakteri yang menyebabkan difteri pertama kali dijelaskan oleh Klebs pada tahun 1883, dan telah diisolasi oleh Loeffler pada tahun 1884,
Pada tahun 1884, Loeffler menyimpulkan bahwa C. diphtheriae menghasilkan toksin larut, dan dengan demikian memberikan gambaran pertama dari eksotoksin bakteri.
Pada 1888, Roux dan Yersin menunjukkan adanya toksin dalam biakan cairan sel C. diphtheriae yang bila disuntikkan ke hewan coba yang sesuai, menyebabkan manifestasi sistemik difteri.
Dua tahun kemudian, von Behring dan Kitasato berhasil mengimunisasi babi guinea- dengan toksin yang dilemahkan /dipanaskan dan menunjukkan bahwa setelah hewan diimunisasi mengandung antitoksin yang mampu melindungi hewan terhadap penyakit. Namun bila diberikan kepada manusia ternyata menyebabkan reaksi lokal yang parah dan tidak dapat digunakan sebagai vaksin.
Pada 1909, Theobald Smith, di AS, menunjukkan bahwa toksin difteri yang telah dinetralkan oleh antitoksin (membentuk Anti-Toxin Toxin kompleks, TAT) tetap imunogenik dan reaksi lokal yang terjadi dapat dihilangkan. Selama beberapa tahun, dimulai sekitar 1910, TAT digunakan untuk imunisasi aktif terhadap difteri. TAT memiliki dua karakteristik yang tidak diinginkan sebagai vaksin,. Pertama, toksin yang digunakan adalah sangat beracun, dan kuantitas yang disuntikkan bisa mengakibatkan toksemia fatal kecuali toksin dinetralkan sepenuhnya oleh antitoksin,. Kedua serum antitoksin berasal dari seekor kuda dimana komponen-komponennya cenderung bersifat alergis..
Pada tahun 1913, Schick merancang tes kulit sebagai alat untuk menentukan kerentanan atau kekebalan terhadap difteri pada manusia. Difteri toksin akan menyebabkan reaksi inflamasi ketika jumlah yang sangat kecil disuntikkan secara intracutan . Schick Test adalah penyuntikan dosis sangat kecil toksin di bawah kulit lengan bawah dan mengevaluasi tempat suntikan setelah 48 jam. Sebuah tes positif (reaksi radang) menunjukkan kelemahan (nonimmunity). Sebuah tes negatif (tidak ada reaksi) menunjukkan kekebalan (antibodi menetralisir toksin).
Pada tahun 1924, Ramon menunjukkan konversi toksin difteri dengan formaldehida supaya tidak beracun, Dia menciptakann salah satu vaksin yang paling aman dan paling pasti sepanjang masa, yaitu toksoid difteri.
Pada tahun 1951, Freeman membuat penemuan luar biasa strain C. diphtheriae yang patogen (toksigen) adalah lisogenik, (yaitu terinfeksi oleh fag Beta subtropis), sedangkan strain terlisogenisasi non avirulent. Selanjutnya, hal itu menunjukkan bahwa gen untuk produksi toksin terletak di fag Beta DNA.
Pada awal 1960-an, Pappenheimer mempelajari efek dari racun dalam biakan sel HeLa dan dalam sistem sel bebas, dan menyimpulkan bahwa toksin menghambat sintesis protein dengan menghalangi transfer asam amino dari tRNA ke rantai polipeptida yang tumbuh di ribosom. Mereka menemukan bahwa toksin bisa dinetralkan oleh antitoksin difteri.
Penyakit Manusia
CDC menjelaskan difteri sebagai penyakit saluran pernapasan atas yang ditandai dengan sakit tenggorokan, demam ringan, dan adanya membran yang menyelubungi tonsil (s), faring, dan / atau hidung.. Sebuah lesi lokal berkembang di saluran pernapasan atas dan menyebabkan luka nekrotik pada sel-sel epitel. Sebagai hasil dari cedera ini, terjadi kebocoran plasma darah ke daerah itu dan membentuk 3 jaringan fibrin yang bertautan dengan dengan pertumbuhan sel C. diphtheriae dengan cepat. Jaringan bermembran, disebut pseudomembrane, bukan hanya sekedar sebagai lesi lokal tapi bisa mengarah ke gangguan pernapasan, bahkan mati lemas.
Gambar 3. Difteri pseudomembrane. CDC.
Basil difteri ini cenderung tidak menyerang jaringan di bawah atau jauh dari permukaan sel epitel di lokasi lesi lokal. Namun, di situs ini mereka menghasilkan toksin yang diserap dan disebarkan melalui saluran getah bening dan darah ke jaringan tubuh penderita. Perubahan degeneratif dalam jaringan, jantung, otot, saraf perifer, adrenal, ginjal, hati dan limpa, mengakibatkan penyakit patologi sistemik.
Patogenisitas Corynebacterium diphtheriae mencakup dua fenomena yang berbeda:
1. Invasi jaringan lokal dari tenggorokan, membutuhkan kolonisasi dan proliferasi bakteri berikutnya. Sedikit yang diketahui tentang mekanisme perlekatan C. diphtheriae, tapi bakteri menghasilkan beberapa jenis pili. Toksin difteri, juga, mungkin terlibat dalam kolonisasi di tenggorokan.
2:. Toxigenesis, produksi toksin bakteri. Toksin difteri eukariotik menyebabkan kematian sel dan jaringan akibat inhibisi sintesis protein dalam sel. Meskipun toksin bertanggung jawab atas gejala-gejala penyakit mematikan, virulensi C. diphtheriae tidak dapat dikaitkan dengan toxigenicity-nya saja. Dan, belum dbisa disimpulkan bahwa toksin difteri memainkan peran penting dalam proses kolonisasi.
Dikenal tiga strain Corynebacterium diphtheriae, gravis, intermedius dan mitis. Semua strain menghasilkan toksin yang identik dan mampu menginfeksi tenggorokan. Perbedaan virulensi antara ketiga strain dapat dijelaskan dengan perbedaan kemampuan mereka dalam menghasilkan derajat toksin dan kuantitas, dan pertumbuhan mereka.
Galur gravis memiliki waktu generasi (in vitro) 60 menit; strain intermedius memiliki waktu generasi sekitar 100 menit, dan mitis memiliki waktu generasi sekitar 180 menit. Strain tumbuh lebih cepat biasanya menghasilkan koloni yang lebih besar pada media pertumbuhan. Dalam tenggorokan (in vivo), tingkat pertumbuhan lebih cepat dan memungkinkan organisme untuk menguras pasokan besi lokal lebih cepat dalam menyerang jaringan, sehingga memungkinkan produksi toksin difteri lebih besar . Juga, jika kinetika produksi toksin mengikuti kinetika pertumbuhan bakteri
Gambar 4 koloni.Corynebacterium diphtheriae Pada agar darah. CDC.
Toxigenicity
Dua faktor yang sangat berpengaruh terhadap kemampuan Corynebacterium diphtheriae menghasilkan toksin difteri: (1) konsentrasi ekstraseluler yang rendah besi dan (2) adanya profag lisogenik dalam kromosom bakteri. Gen untuk produksi toksin terjadi pada kromosom dari profag, tetapi sebuah protein represor bakteri mengontrol ekspresi gen ini. represor diaktifkan oleh besi, dan dalam cara yang sama besi mempengaruhi produksi toksin, Toksin hanya disintesis oleh bakteri lisogenik dalam kondisi kekurangan zat besi.
Peran besi. dalam media buatan. Faktor terpenting dalam mengontrol produksi toksin adalah konsentrasi besi anorganik (Fe + + atau Fe + + +) yang terkandung dalam medium. Toksin disintesis dalam jumlah besar hanya setelah pemberian eksogen besi dikurangi (ini penting dalam industri produksi racun untuk membuat toksoid. Di bawah kondisi kelaparan besi, C. diphtheriae akan mensintesis toksin difteri sebesar 5% dari total protein). Agaknya, fenomena ini terjadi di invivo juga. bakteri tidak dapat menghasilkan jumlah maksimal dari toksin sampai pasokan besi dalam jaringan pada saluran pernafasan atas telah habis. Ini adalah aturan produksi racun dalam bakteri yang sebagian dikendalikan oleh besi. Gen tox diatur oleh mekanisme kontrol negatif dimana molekul represor, produk dari gen DtxR, diaktifkan dengan besi. Mengikat represor aktif untuk operator gen tox dan mencegah transkripsi. Ketika besi dihapus dari represor (dalam kondisi pertumbuhan keterbatasan besi), derepression terjadi, represor ini dilemahkan dan transkripsi gen tox dapat terjadi. Besi disebut sebagai corepressor yang mana diperlukan untuk represi gen toksin.
Peran B-fag. Hanya strain Corynebacterium diphtheriae yang terlisogenisasi oleh fag Beta tertentu yang menghasilkan toksin difteri. CRMs memiliki panjang rantai lebih pendek dari molekul toksin difteri tapi bereaksi silang dengan antitoxins difteri karena kesamaan antigenik mereka.. CRMs diyakini bahwa gen tox berada pada kromosom fag daripada kromosom bakteri.
Meskipun gen tox bukan bagian dari kromosom bakteri, regulasi produksi toksin berada di bawah kontrol bakteri
Gambar 5. Fag Beta yang dikode oleh gen tox untuk toksin difteri.
Tidak ada bukti yang menunjukkan peran penting dari toksin dalam siklus hidup organisme. Sejak imunisasi massal terhadap difteri telah dipraktikkan, penyakit ini telah hampir menghilang, dan C. diphtheriae tidak lagi menjadi komponen flora normal dari tenggorokan manusia dan faring. Mungkin toksin masih memainkan peran penting dalam kolonisasi tenggorokan pada orang nonimmune. Dan, sebagai konsekuensi dari imunisasi lengkap, strain toksigen telah menjadi hampir punah.
Gambar 6. Toxin Difteri (DTx) Monomer). (A merah adalah domain katalitik; B (kuning) adalah domain yang mengikat sel reseptor untuk lampiran; T (biru) adalah domain hidrofobik bertanggung jawab untuk masuk ke dalam membran endosome untuk mengamankan pelepasan Protein A. yang digambarkan dalam "" konfigurasi tertutup.
Gambar 7. Mekanisme kerja toksin Difteri DTxA.
Gambar 8. Penyerapan dan aktivitas dari toksin difteri dalam sel eukariotik.
Kekebalan terhadap Difteri
Kekebalan terhadap difteri Acquired, atau antibodi toksin (antitoksin), kekebalan pasif di dalam rahim diperoleh transplacentally dan dapat bertahan selama 1 atau 2 tahun setelah kelahiran. Di daerah di mana difteri adalah endemik dan imunisasi massal tidak dilakukan, kebanyakan anak muda sangat rentan terhadap infeksi. Mungkin, imunitas aktif dapat diproduksi akibat infeksi ringan pada bayi yang masih mempunyai antibodi dari ibu, dan pada orang dewasa yang terinfeksi dengan strain virulensi rendah (infeksi inapparent).
Individu yang telah sepenuhnya pulih dari difteri dapat terus sebagai pembawa organisme di tenggorokan atau hidung selama beberapa minggu atau bahkan berbulan-bulan.
Karena tingginya tingkat kerentanan anak-anak, imunisasi buatan pada usia dini secara universal dianjurkan. Toksoid diberikan dalam 2 atau 3 dosis ( terpisah1 bulan ) untuk imunisasi dasar pada usia 3 - 4 bulan. Suntikan booster harus diberikan sekitar setahun kemudian, dan ia dianjurkan untuk melanjutkan beberapa suntikan booster selama masa kanak-kanak. Biasanya, bayi diimunisasi dengan vaksin trivalen berisi toksoid difteri, vaksin pertusis, dan tetanus toksoid (DPT atau DTaP vaksin).
Persentase peningkatan kasus difteri pada orang dewasa mmungkin bahwa banyak orang dewasa tidak dilindungi terhadap difteri, karena mereka tidak menerima imunisasi penguat dalam sepuluh tahun terakhir. Situasi yang sama seperti dengan tetanus.
PHOTO :
Fotomikrograf ini menggambarkan sejumlah bakteri Gram-positif Corynebacterium diphtheriae, yang telah dicat menggunakan teknik biru metilen. Spesimen diambil dari biakan miring Pai's.
Koloni C.difteri
Corynebacterium diphtheriae
Corynebacteria adalah bakteri Gram-positif, aerobik, nonmotile, berbentuk batang diklasifikasikan sebagai Actinobacteria. Corynebacteria membentuk karakteristik yang tidak teratur, mereka mengalami gertakan gerakan setelah pembelahan sel, yang membuat mereka ke dalam bentuk-bentuk karakteristik yang mirip huruf Cina atau pagar.
Genus Corynebacterium terdiri dari berbagai kelompok bakteri patogen termasuk pada hewan dan tanaman, serta saprophytes. Beberapa Corynebacteria merupakan bagian dari flora normal manusia, terdapay di hampir semua situs anatomi, terutama kulit dan mukosa hidung.. Spesies yang paling dikenal dan paling banyak dipelajari adalah Corynebacterium diphtheriae, agen penyebab dari penyakit difteri.
Gambar 1. Sel. Corynebacterium, penampilan ini disebabkan oleh adanya inklusi polifosfat yang disebut butiran metachromatic. Perhatikan juga susunan sel. "karakteristik huruf Cina- "
Difteri adalah penyakit saluran pernapasan atas yang ditandai dengan sakit tenggorokan, demam rendah, dan membran putih abu-abu (disebut pseudomembrane pada tonsil, faring, dan / atau rongga hidung. Toksin Difteri. diproduksi oleh C. diphtheriae, dapat menyebabkan miokarditis, polyneuritis, dan efek beracun sistemik lainnya. Penyebaran penyakit melalui kontak fisik langsung atau cairan pernapasan aerosol dari individu yang terinfeksi. Vaksin DPT. terbukti efektif menurunkan insiden penyakit difteri.
Difteri adalah penyakit yang serius, dengan tingkat kematian antara 5% dan 10%. Pada anak-anak di bawah 5 tahun dan orang dewasa lebih dari 40 tahun, tingkat kematian mungkin sebanyak 20%. Wabah, meskipun sangat jarang, masih terjadi di seluruh dunia, bahkan di negara-negara maju.
Sejarah dan Latar Belakang
Hippocrates memberikan penjelasan klinis pertama dari difteri pada abad ke-4 SM
Pada abad ke-17, epidemi difteri menyapu Eropa; di Spanyol penyakit dikenal sebagai " El garatillo " (Sang pencekik "), di Italia dan Sisilia dikenal sebagai" penyakit tenggorokan ".
Pada abad ke-18, penyakit ini mencapai koloni Amerika di mana, sekitar tahun 1735 sering kali, seluruh keluarga dalam beberapa minggu meninggal karena penyakit ini .
Bakteri yang menyebabkan difteri pertama kali dijelaskan oleh Klebs pada tahun 1883, dan telah diisolasi oleh Loeffler pada tahun 1884,
Pada tahun 1884, Loeffler menyimpulkan bahwa C. diphtheriae menghasilkan toksin larut, dan dengan demikian memberikan gambaran pertama dari eksotoksin bakteri.
Pada 1888, Roux dan Yersin menunjukkan adanya toksin dalam biakan cairan sel C. diphtheriae yang bila disuntikkan ke hewan coba yang sesuai, menyebabkan manifestasi sistemik difteri.
Dua tahun kemudian, von Behring dan Kitasato berhasil mengimunisasi babi guinea- dengan toksin yang dilemahkan /dipanaskan dan menunjukkan bahwa setelah hewan diimunisasi mengandung antitoksin yang mampu melindungi hewan terhadap penyakit. Namun bila diberikan kepada manusia ternyata menyebabkan reaksi lokal yang parah dan tidak dapat digunakan sebagai vaksin.
Pada 1909, Theobald Smith, di AS, menunjukkan bahwa toksin difteri yang telah dinetralkan oleh antitoksin (membentuk Anti-Toxin Toxin kompleks, TAT) tetap imunogenik dan reaksi lokal yang terjadi dapat dihilangkan. Selama beberapa tahun, dimulai sekitar 1910, TAT digunakan untuk imunisasi aktif terhadap difteri. TAT memiliki dua karakteristik yang tidak diinginkan sebagai vaksin,. Pertama, toksin yang digunakan adalah sangat beracun, dan kuantitas yang disuntikkan bisa mengakibatkan toksemia fatal kecuali toksin dinetralkan sepenuhnya oleh antitoksin,. Kedua serum antitoksin berasal dari seekor kuda dimana komponen-komponennya cenderung bersifat alergis..
Pada tahun 1913, Schick merancang tes kulit sebagai alat untuk menentukan kerentanan atau kekebalan terhadap difteri pada manusia. Difteri toksin akan menyebabkan reaksi inflamasi ketika jumlah yang sangat kecil disuntikkan secara intracutan . Schick Test adalah penyuntikan dosis sangat kecil toksin di bawah kulit lengan bawah dan mengevaluasi tempat suntikan setelah 48 jam. Sebuah tes positif (reaksi radang) menunjukkan kelemahan (nonimmunity). Sebuah tes negatif (tidak ada reaksi) menunjukkan kekebalan (antibodi menetralisir toksin).
Pada tahun 1924, Ramon menunjukkan konversi toksin difteri dengan formaldehida supaya tidak beracun, Dia menciptakann salah satu vaksin yang paling aman dan paling pasti sepanjang masa, yaitu toksoid difteri.
Pada tahun 1951, Freeman membuat penemuan luar biasa strain C. diphtheriae yang patogen (toksigen) adalah lisogenik, (yaitu terinfeksi oleh fag Beta subtropis), sedangkan strain terlisogenisasi non avirulent. Selanjutnya, hal itu menunjukkan bahwa gen untuk produksi toksin terletak di fag Beta DNA.
Pada awal 1960-an, Pappenheimer mempelajari efek dari racun dalam biakan sel HeLa dan dalam sistem sel bebas, dan menyimpulkan bahwa toksin menghambat sintesis protein dengan menghalangi transfer asam amino dari tRNA ke rantai polipeptida yang tumbuh di ribosom. Mereka menemukan bahwa toksin bisa dinetralkan oleh antitoksin difteri.
Penyakit Manusia
CDC menjelaskan difteri sebagai penyakit saluran pernapasan atas yang ditandai dengan sakit tenggorokan, demam ringan, dan adanya membran yang menyelubungi tonsil (s), faring, dan / atau hidung.. Sebuah lesi lokal berkembang di saluran pernapasan atas dan menyebabkan luka nekrotik pada sel-sel epitel. Sebagai hasil dari cedera ini, terjadi kebocoran plasma darah ke daerah itu dan membentuk 3 jaringan fibrin yang bertautan dengan dengan pertumbuhan sel C. diphtheriae dengan cepat. Jaringan bermembran, disebut pseudomembrane, bukan hanya sekedar sebagai lesi lokal tapi bisa mengarah ke gangguan pernapasan, bahkan mati lemas.
Gambar 3. Difteri pseudomembrane. CDC.
Basil difteri ini cenderung tidak menyerang jaringan di bawah atau jauh dari permukaan sel epitel di lokasi lesi lokal. Namun, di situs ini mereka menghasilkan toksin yang diserap dan disebarkan melalui saluran getah bening dan darah ke jaringan tubuh penderita. Perubahan degeneratif dalam jaringan, jantung, otot, saraf perifer, adrenal, ginjal, hati dan limpa, mengakibatkan penyakit patologi sistemik.
Patogenisitas Corynebacterium diphtheriae mencakup dua fenomena yang berbeda:
1. Invasi jaringan lokal dari tenggorokan, membutuhkan kolonisasi dan proliferasi bakteri berikutnya. Sedikit yang diketahui tentang mekanisme perlekatan C. diphtheriae, tapi bakteri menghasilkan beberapa jenis pili. Toksin difteri, juga, mungkin terlibat dalam kolonisasi di tenggorokan.
2:. Toxigenesis, produksi toksin bakteri. Toksin difteri eukariotik menyebabkan kematian sel dan jaringan akibat inhibisi sintesis protein dalam sel. Meskipun toksin bertanggung jawab atas gejala-gejala penyakit mematikan, virulensi C. diphtheriae tidak dapat dikaitkan dengan toxigenicity-nya saja. Dan, belum dbisa disimpulkan bahwa toksin difteri memainkan peran penting dalam proses kolonisasi.
Dikenal tiga strain Corynebacterium diphtheriae, gravis, intermedius dan mitis. Semua strain menghasilkan toksin yang identik dan mampu menginfeksi tenggorokan. Perbedaan virulensi antara ketiga strain dapat dijelaskan dengan perbedaan kemampuan mereka dalam menghasilkan derajat toksin dan kuantitas, dan pertumbuhan mereka.
Galur gravis memiliki waktu generasi (in vitro) 60 menit; strain intermedius memiliki waktu generasi sekitar 100 menit, dan mitis memiliki waktu generasi sekitar 180 menit. Strain tumbuh lebih cepat biasanya menghasilkan koloni yang lebih besar pada media pertumbuhan. Dalam tenggorokan (in vivo), tingkat pertumbuhan lebih cepat dan memungkinkan organisme untuk menguras pasokan besi lokal lebih cepat dalam menyerang jaringan, sehingga memungkinkan produksi toksin difteri lebih besar . Juga, jika kinetika produksi toksin mengikuti kinetika pertumbuhan bakteri
Gambar 4 koloni.Corynebacterium diphtheriae Pada agar darah. CDC.
Toxigenicity
Dua faktor yang sangat berpengaruh terhadap kemampuan Corynebacterium diphtheriae menghasilkan toksin difteri: (1) konsentrasi ekstraseluler yang rendah besi dan (2) adanya profag lisogenik dalam kromosom bakteri. Gen untuk produksi toksin terjadi pada kromosom dari profag, tetapi sebuah protein represor bakteri mengontrol ekspresi gen ini. represor diaktifkan oleh besi, dan dalam cara yang sama besi mempengaruhi produksi toksin, Toksin hanya disintesis oleh bakteri lisogenik dalam kondisi kekurangan zat besi.
Peran besi. dalam media buatan. Faktor terpenting dalam mengontrol produksi toksin adalah konsentrasi besi anorganik (Fe + + atau Fe + + +) yang terkandung dalam medium. Toksin disintesis dalam jumlah besar hanya setelah pemberian eksogen besi dikurangi (ini penting dalam industri produksi racun untuk membuat toksoid. Di bawah kondisi kelaparan besi, C. diphtheriae akan mensintesis toksin difteri sebesar 5% dari total protein). Agaknya, fenomena ini terjadi di invivo juga. bakteri tidak dapat menghasilkan jumlah maksimal dari toksin sampai pasokan besi dalam jaringan pada saluran pernafasan atas telah habis. Ini adalah aturan produksi racun dalam bakteri yang sebagian dikendalikan oleh besi. Gen tox diatur oleh mekanisme kontrol negatif dimana molekul represor, produk dari gen DtxR, diaktifkan dengan besi. Mengikat represor aktif untuk operator gen tox dan mencegah transkripsi. Ketika besi dihapus dari represor (dalam kondisi pertumbuhan keterbatasan besi), derepression terjadi, represor ini dilemahkan dan transkripsi gen tox dapat terjadi. Besi disebut sebagai corepressor yang mana diperlukan untuk represi gen toksin.
Peran B-fag. Hanya strain Corynebacterium diphtheriae yang terlisogenisasi oleh fag Beta tertentu yang menghasilkan toksin difteri. CRMs memiliki panjang rantai lebih pendek dari molekul toksin difteri tapi bereaksi silang dengan antitoxins difteri karena kesamaan antigenik mereka.. CRMs diyakini bahwa gen tox berada pada kromosom fag daripada kromosom bakteri.
Meskipun gen tox bukan bagian dari kromosom bakteri, regulasi produksi toksin berada di bawah kontrol bakteri
Gambar 5. Fag Beta yang dikode oleh gen tox untuk toksin difteri.
Tidak ada bukti yang menunjukkan peran penting dari toksin dalam siklus hidup organisme. Sejak imunisasi massal terhadap difteri telah dipraktikkan, penyakit ini telah hampir menghilang, dan C. diphtheriae tidak lagi menjadi komponen flora normal dari tenggorokan manusia dan faring. Mungkin toksin masih memainkan peran penting dalam kolonisasi tenggorokan pada orang nonimmune. Dan, sebagai konsekuensi dari imunisasi lengkap, strain toksigen telah menjadi hampir punah.
Gambar 6. Toxin Difteri (DTx) Monomer). (A merah adalah domain katalitik; B (kuning) adalah domain yang mengikat sel reseptor untuk lampiran; T (biru) adalah domain hidrofobik bertanggung jawab untuk masuk ke dalam membran endosome untuk mengamankan pelepasan Protein A. yang digambarkan dalam "" konfigurasi tertutup.
Gambar 7. Mekanisme kerja toksin Difteri DTxA.
Gambar 8. Penyerapan dan aktivitas dari toksin difteri dalam sel eukariotik.
Kekebalan terhadap Difteri
Kekebalan terhadap difteri Acquired, atau antibodi toksin (antitoksin), kekebalan pasif di dalam rahim diperoleh transplacentally dan dapat bertahan selama 1 atau 2 tahun setelah kelahiran. Di daerah di mana difteri adalah endemik dan imunisasi massal tidak dilakukan, kebanyakan anak muda sangat rentan terhadap infeksi. Mungkin, imunitas aktif dapat diproduksi akibat infeksi ringan pada bayi yang masih mempunyai antibodi dari ibu, dan pada orang dewasa yang terinfeksi dengan strain virulensi rendah (infeksi inapparent).
Individu yang telah sepenuhnya pulih dari difteri dapat terus sebagai pembawa organisme di tenggorokan atau hidung selama beberapa minggu atau bahkan berbulan-bulan.
Karena tingginya tingkat kerentanan anak-anak, imunisasi buatan pada usia dini secara universal dianjurkan. Toksoid diberikan dalam 2 atau 3 dosis ( terpisah1 bulan ) untuk imunisasi dasar pada usia 3 - 4 bulan. Suntikan booster harus diberikan sekitar setahun kemudian, dan ia dianjurkan untuk melanjutkan beberapa suntikan booster selama masa kanak-kanak. Biasanya, bayi diimunisasi dengan vaksin trivalen berisi toksoid difteri, vaksin pertusis, dan tetanus toksoid (DPT atau DTaP vaksin).
Persentase peningkatan kasus difteri pada orang dewasa mmungkin bahwa banyak orang dewasa tidak dilindungi terhadap difteri, karena mereka tidak menerima imunisasi penguat dalam sepuluh tahun terakhir. Situasi yang sama seperti dengan tetanus.
PHOTO :
Fotomikrograf ini menggambarkan sejumlah bakteri Gram-positif Corynebacterium diphtheriae, yang telah dicat menggunakan teknik biru metilen. Spesimen diambil dari biakan miring Pai's.
Koloni C.difteri
Kultur BakTeri AnAEROB
Kultur bakteri anaerob adalah metode yang digunakan untuk menumbuhkan spesimen klinis secara anaerob . Bakteri anaerob Obligat hanya bisa hidup tanpa adanya oksigen, anaerob obligat akan hancur saat kontak dengan atmosfer selama 10 menit. Beberapa anaerob ada yang toleran terhadap sejumlah kecil oksigen. Anaerob fakultatif adalah organisme yang dapat tumbuh dengan atau tanpa oksigen. Metode mendapatkan spesimen untuk kultur anaerobik dan prosedur biakan anaerob harus dilakukan untuk memastikan bahwa organisme terlindung dari oksigen.
Tujuan
Biakan bakteri anaerobik dilakukan untuk mengidentifikasi bakteri yang dapat menyebabkan infeksi pada manusia yang tumbuh hanya dalam ketiadaan oksigen . Infeksi bakteri anaerob dapat menyebabkan konsekuensi serius seperti amputasi , kegagalan organ, sepsis, meningitis, dan kematian. Biakan diperlukan untuk mengidentifikasi patogen anaerobik dengan benar dan pemilihan antibiotik yang efektif.
Tindakan pencegahan
Sangat penting bahwa penyedia layanan kesehatan untuk mendapatkan sampel klinis untuk dibiakkan melalui teknik aseptik . Bakteri anaerob umumnya ditemukan pada selaput lendir dan situs lainnya seperti vagina dan rongga mulut. Oleh karena itu, spesimen yang mungkin terkontaminasi dengan organisme ini tidak dianjurkan untuk dibiakkan (misalnya, vagina atau usap tenggorokan). Beberapa jenis spesimen harus selalu dibiakkan secara anaerob jika dicurigai ada infeksi . Ini termasuk abses, gigitan, darah, cairan tulang punggung / cairan otak dan cairan tubuh exudative, luka dalam, dan jaringan mati. Spesimen harus dilindungi dari oksigen selama pengumpulan dan transportasi kemudian harus dibawa ke laboratorium segera.
Deskripsi
Anaerob biasanya ditemukan di area tubuh tertentu , tetapi dapat mengakibatkan infeksi serius ketika mereka memiliki akses ke cairan tubuh yang biasanya steril atau ke jaringan dalam yang kurang oksigen. Beberapa anaerob biasanya tinggal di celah-celah kulit, di hidung, mulut, tenggorokan, usus, dan vagina. Cedera pada jaringan tersebut (yaitu, luka, luka tusuk, atau trauma) terutama pada atau berdekatan dengan membran mukosa memungkinkan bakteri anaerob masuk ke daerah tubuh yang steril tersebut dan menjadi penyebab utama infeksi bakteri anaerob. Sumber kedua infeksi anaerob terjadi akibat terpaparnya bagian tubuh yang secara normal steril dengan spora bakteri. Bakteri anaerob tinggal di tanah dan air, memproduksi spora, Spora tersebut dapat masuk melalui luka, terutama tusukan. Infeksi Anaerobik paling sering ditemukan pada orang yang imunosupresif, pada mereka yang baru dirawat dengan antibiotik spektrum luas, dan pada orang-orang yang memiliki cedera jaringan membusuk pada atau dekat membran lendir, terutama pada situs yang berbau busuk.
Beberapa spesimen yang patut dibiakkan secara anaerob adalah:
darah
empedu
sumsum tulang
cairan serebrospinal
aspirasi langsung paru-paru
biopsi jaringan dari suatu situs yang biasanya steril
cairan dari situs yang biasanya steril
abses gigi
abses abdominal atau panggul
luka pisau, tembak, atau bedah
terbakar yang parah
Beberapa spesimen yang tidak cocok untuk biakan anaerob meliputi:
discharge tenggorokan , batuk (dahak)
usap dubur
usap hidung atau tenggorokan
usap uretra
urin yang keluar lewat urethra
Koleksi Spesimen
Kunci efektif membiakkan bakteri anaerob termasuk mengumpulkan spesimen bebas kontaminasi dan melindunginya dari paparan oksigen atau. biakan bakteri anaerob harus diperoleh dari sebuah situs yang tepat tanpa terkontaminasi sampel yang berdekatan dengan bakteri dari kulit lendir, membran, jaringan. Kapas harus dihindari ketika mengambil spesimen untuk kultur anaerob karena serat kapas dapat merugikan anaerob. Abses atau cairan bisa disedot dengan menggunakan jarum steril yang kemudian ditutup rapat untuk mencegah masuknya udara. Sampel jaringan harus ditempatkan ke dalam kantong "degassed" dan disegel, atau dimasukkan botol bertutup ulir dan divacuum atas dimasukkan ke dalam botol berisi medium kultur prereduced bebas -oksigen dan ditutup rapat. Spesimen harus dipindah secepat mungkin ke media kultur yang telah disiapkan.
Kultur/biakan
Biakan harus ditempatkan dalam suatu lingkungan yang bebas oksigen, pada 95 ° F (35 ° C) setidaknya selama 48 jam sebelum diperiksa pertumbuhannya..
Pewarnaan Gram dilakukan pada spesimen pada saat dibiakkan. Infeksi dapat disebabkan oleh bakteri aerobik atau anaerobik atau campuran keduanya, beberapa infeksi memiliki probabilitas tinggi disebabkan oleh bakteri anaerob. Infeksi ini termasuk abses otak, abses paru-paru, aspirasi pneumonia , dan infeksi gigi. Organisme anaerobik sering dapat diduga karena banyak anaerob memiliki morfologi mikroskopis yang karakteristik . Sebagai contoh, Bacteroides spp. adalah batang gram-negatif yang pleomorphic (variabel dalam ukuran dan bentuk) dan menunjukkan pewarnaan bipolar yang tidak teratur Fusobacterium spp.. sering pucat berbentuk batang gram-negatif memiliki spindle . Clostridium spp.. adalah batang besar gram positif yang membentuk spora. Lokasi spora (pusat, subterminal, terminal, atau tidak ada) adalah karakteristik diferensial yang berguna. Adanya pertumbuhan, toleransi oksigen, dan hasil Gram stain cukup untuk menetapkan diagnosis awal infeksi anaerob dan memulai perawatan dengan obat antibiotik yang sesuai untuk sebagian besar anaerob seperti klindamisin, metronidazol, atau vankomisin.
Gram-negatif anaerob dan beberapa infeksi yang mereka hasilkan meliputi genera berikut:
Bacteroides (anaerob yang biasa ditemukan dalam biakan pada infeksi intra-abdomen, abses rektal, infeksi jaringan lunak, infeksi hati)
Fusobacterium (abses, infeksi luka, dan infeksi paru intrakranial)
Porphyromonas (aspirasi pneumonia , periodontitis)
Prevotella (infeksi intra-abdomen, infeksi jaringan lunak)
Gram-positif anaerob adalah sebagai berikut:
Actinomyces (kepala, leher, infeksi perut; aspirasi pneumonia )
Bifidobacterium (infeksi telinga, infeksi perut)
Clostridium (gas, gangren, keracunan makanan, tetanus, kolitis pseudomembranosa)
Peptostreptococcus (oral, pernapasan, dan infeksi intra-abdomen)
Propionibacterium (infeksi shunt)
Identifikasi anaerob sangat kompleks, dan laboratorium mungkin menggunakan sistem identifikasi parsial yang berbeda. tujuan. Misalnya, ada enam spesies dari genus Bacteroides yang dapat diidentifikasi sebagai kelompok Bacteroides fragilis daripada diidentifikasi secara individual. Organisme diidentifikasi berdasar kolonial dan morfologi mikroskopis mereka , pertumbuhan pada media selektif, toleransi oksigen, dan karakteristik biokimia. Ini termasuk fermentasi gula, kelarutan empedu, esculin, pati, dan hidrolisis gelatin, kasein dan lysis gel, katalase, lipase, lecithinase, dan produksi indol, reduksi nitrat, asam lemak volatil yang ditentukan dengan kromatografi gas, dan kerentanan terhadap antibiotik. Profil kerentanan antibiotik ditentukan oleh microtube metode dilusi . Banyak spesies anaerob yang resisten terhadap penisilin, dan ada pula yang tahan terhadap klindamisin dan antibiotik lain yang biasa. digunakan
Diagnosis / Persiapan
Penyedia perawatan kesehatan harus berhati-hati untuk mengumpulkan spesimen-bebas kontaminasi. Semua prosedur harus dilakukan secara aseptik. Perawat profesional kesehatan yang mengumpulkan spesimen harus siap untuk mengambil dua sampel, satu untuk biakan anaerob dan satu untuk biakan aerobik, karena tidak diketahui apakah patogen dapat tumbuh dengan atau tanpa oksigen. Selain itu, perawat kesehatan profesional harus mencatat antibiotik yang diberikan ke pasien saat pengambilan sampel dan kondisi medis lain yang dapat mempengaruhi pertumbuhan bakteri.
Rehabilitasi
Dalam sampling darah vena untuk biakan darah anaerob, langsung tekan harus diterapkan ke situs tusukan vena selama beberapa menit atau sampai pendarahan berhenti. Sebuah perban perekat dapat diterapkan, . Jika terjadi bengkak atau memar es dapat diterapkan ke situs. Untuk koleksi spesimen selain darah, pasien dan situs koleksi harus dipantau untuk setiap komplikasi setelah prosedur.
Risiko
Perhatian khusus harus dilakukan oleh tim kesehatan, mendapatkan, mengangkut, dan mempersiapkan spesimen untuk kultur anaerobik. metodologi yang buruk mungkin memperlamban identifikasi bakteri, menyebabkan kondisi pasien memburuk, dan mungkin memerlukan pasien untuk memberikan sampel lebih daripada yang akan diperlukan. Pasien mungkin mengalami memar, ketidaknyamanan, atau bengkak di situs koleksi ketika jaringan, darah, atau cairan lainnya diperoleh.
Hasil
Hasil negatif akan menunjukkan tidak ada pertumbuhan patogen dalam sampel. Hasil positif akan menunjukkan pertumbuhan, identifikasi setiap bakteri, dan uji kepekaan antibiotik
Pendidikan Pasien
Seorang anggota tim perawat kesehatan harus menjelaskan prosedur koleksi spesimen untuk pasien. Jika pasien sakit parah, anggota tim harus menjelaskan prosedur kepada anggota keluarga pasien. Pasien dan atau keluarganya dia harus memahami bahwa karena bakteri membutuhkan waktu untuk tumbuh di laboratorium, mungkin diperlukan beberapa hari untuk identifikasi bakteri.
PHOTO :
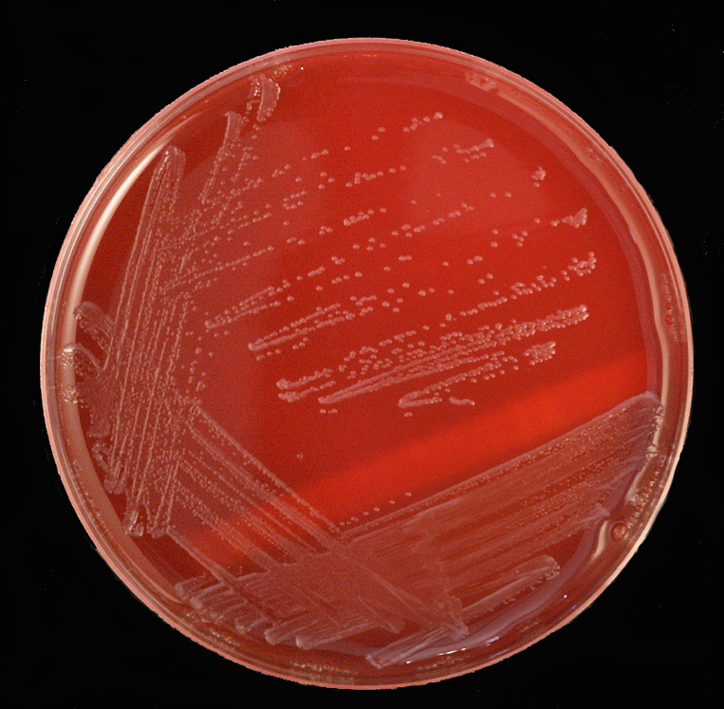
Bacteroides
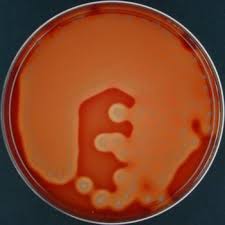
Fusobacterium
Porphyromonas
Prevotella
Actinomyces
Bifidobacterium
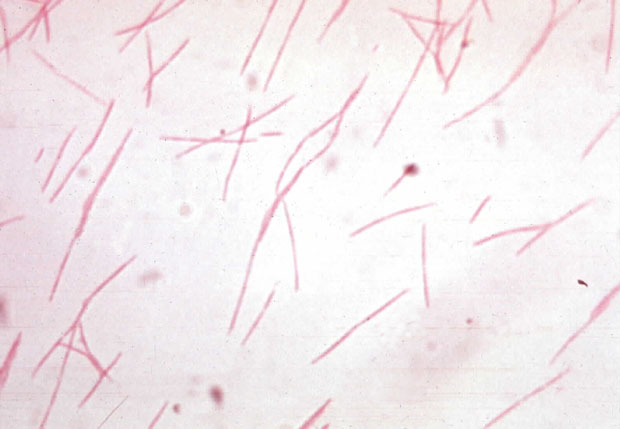
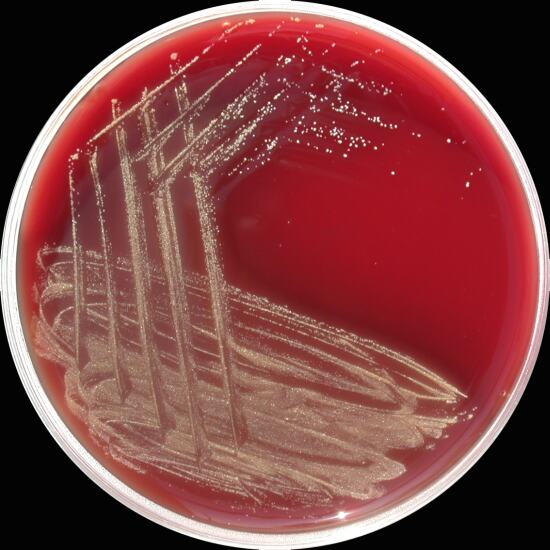
Clostridium
C.botulinum


Clostridium tetani Clostridium difficile
 C. perfringens
C. perfringensPeptostreptococcus
Propionibacterium
Sumber Daya
BUKU
Anel, Ramon L. and R. Phillip Dellinger. "Sepsis and Bacteremia." In Conn's Current Therapy 2001, edited by Robert E. Rakel and Edward T. Bope. Philadelphia: W.B. Saunders Company, 2001, pp.56–62.
Fischbach, Frances. "Blood Cultures." In A Manual of Laboratory & Diagnostic Tests. 6th ed. Philadelphia: Lippincott Williams & Wilkins, 2000, pp.542–545.
Henry, J.B. Clinical Diagnosis and Management by Laboratory Methods. 20th ed. New York: W.B.Saunders Company, 2001.
Wallach, Jacques. Interpretation of Diagnostic Tests. 7th ed. Philadelphia, PA: Lippincott Williams & Wilkens, 2000.
Langganan:
Komentar (Atom)
BIAKAN TINJA
BIAKAN TINJA Tinja normal mengandung berbagai spesies bakteri, beberapa di antaranya potensial patogen. Pemeriksaan bakteriologis berguna u...